PNAS: Identifican las células clave para prevenir la aterosclerosis en el síndrome de progeria
La eliminación de progerina en células de músculo liso vascular, pero no en células endoteliales, previene la aterosclerosis asociada al síndrome de progeria de Hutchinson-Gilford (HGPS)
El síndrome de progeria de Hutchinson-Gilford (HGPS) es una enfermedad genética extremadamente rara que afecta a 1 de cada 20 millones de personas –se estima que afecta a menos de 400 niños en todo el mundo- y se caracteriza por inducir envejecimiento acelerado, aterosclerosis severa y muerte prematura a una edad media aproximada de 15 años. Aunque los pacientes de HGPS normalmente no presentan los típicos factores de riesgo cardiovascular (hipercolesterolemia, obesidad, tabaquismo, etc.), su principal causa de muerte son complicaciones de la aterosclerosis, como el infarto de miocardio, accidente cerebrovascular o insuficiencia cardíaca. Dado que actualmente no existe cura para la progeria, es urgente desarrollar nuevas terapias que prevengan la aterosclerosis y otras alteraciones vasculares asociadas a la enfermedad para aumentar la esperanza de vida de los pacientes.
La causa genética de HGPS es una mutación en el gen LMNA que provoca la expresión de progerina, una versión mutante de la proteína nuclear lamina A que induce numerosos efectos dañinos a nivel celular y del organismo.
Estudios recientes realizados en modelos animales de este síndrome han demostrado que es posible corregir dicha mutación mediante edición génica, y que la consiguiente eliminación de progerina y recuperación de la expresión de lamina A mejora las alteraciones características de HGPS y prolonga la esperanza de vida.
Con el fin de optimizar la terapia génica para el posible tratamiento de pacientes con progeria, es importante identificar los tipos celulares en los que la eliminación de progerina produce más beneficios.
Para abordar esta pregunta, el laboratorio del Dr. Vicente Andrés, del Centro Nacional de Investigaciones Cardiovasculares Carlos III (CNIC) y del CIBER de Enfermedades Cardiovasculares (CIBERCV), había generado previamente el ratón HGPSrev. Los resultados de este estudio se publicaron en la revista Circulation y señalaban a las células de músculo liso vascular como una posible diana terapéutica para combatir la aterosclerosis prematura en la progeria.
“Este modelo de progeria expresa progerina y carece de lamina A en todo el organismo, y permite la eliminación de progerina y la restauración de lamina A en tipos celulares específicos y en diferentes fases de la enfermedad”, explica el Dr. Andrés.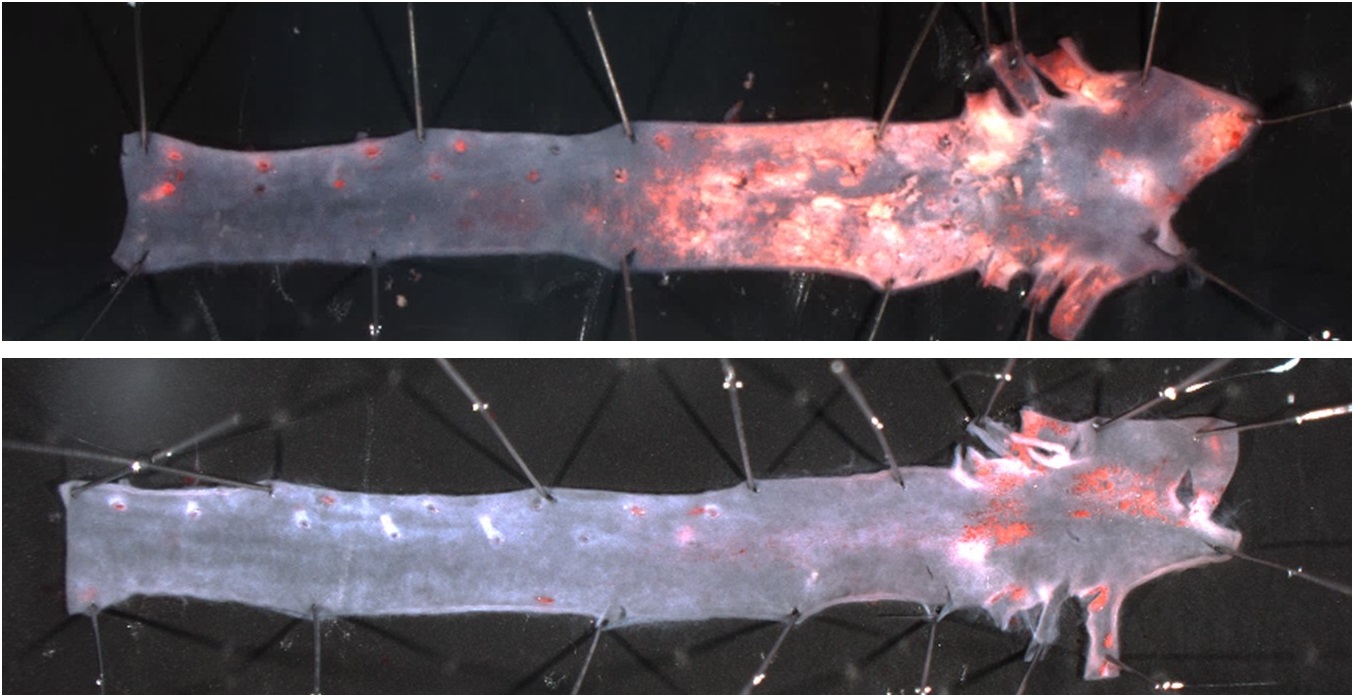
Ahora en un trabajo que se publica en The Proceedings of the National Academy of Sciences (PNAS), utilizando los ratones HGPSrev, Ignacio Benedicto, del Centro de Investigaciones Biológicas Margarita Salas-CSIC, y el grupo del Dr. Vicente Andrés, en colaboración con la Universidad de Oviedo y la Queen Mary University of London (Reino Unido), han estudiado si la aterosclerosis asociada a HGPS puede evitarse mediante la supresión de progerina y la restauración de lamina A en células endoteliales o en células de músculo liso vascular, “dos tipos celulares de la pared arterial que juegan un papel clave en el desarrollo de aterosclerosis convencional”, explica el Dr. Benedicto.
Los investigadores descubrieron que la eliminación de progerina en células endoteliales no reportaba ningún beneficio. En estos ratones se observó aterosclerosis, fibrosis arterial, inflamación vascular, pérdida de peso y muerte prematura de manera idéntica a los ratones con expresión de progerina en todo el organismo. Por el contrario, aquellos ratones HGPSrev a los que se eliminó progerina en células de músculo liso vascular mostraron un nivel de aterosclerosis idéntico al desarrollado por ratones control sin expresión de progerina, y tampoco tuvieron exceso de fibrosis arterial e inflamación vascular.
“Estos resultados sugieren que la corrección de la mutación causante de HGPS en células de músculo liso vascular podría ser suficiente para producir un beneficio terapéutico significativo”, subraya el Dr. Benedicto.
El Dr. Andrés concluye que “una estrategia de este tipo probablemente requeriría dosis más bajas de reactivos de edición génica que las necesarias para la eliminación de progerina en todo el organismo, lo que podría aumentar la posibilidad de desarrollar futuras aplicaciones clínicas más eficaces y seguras”.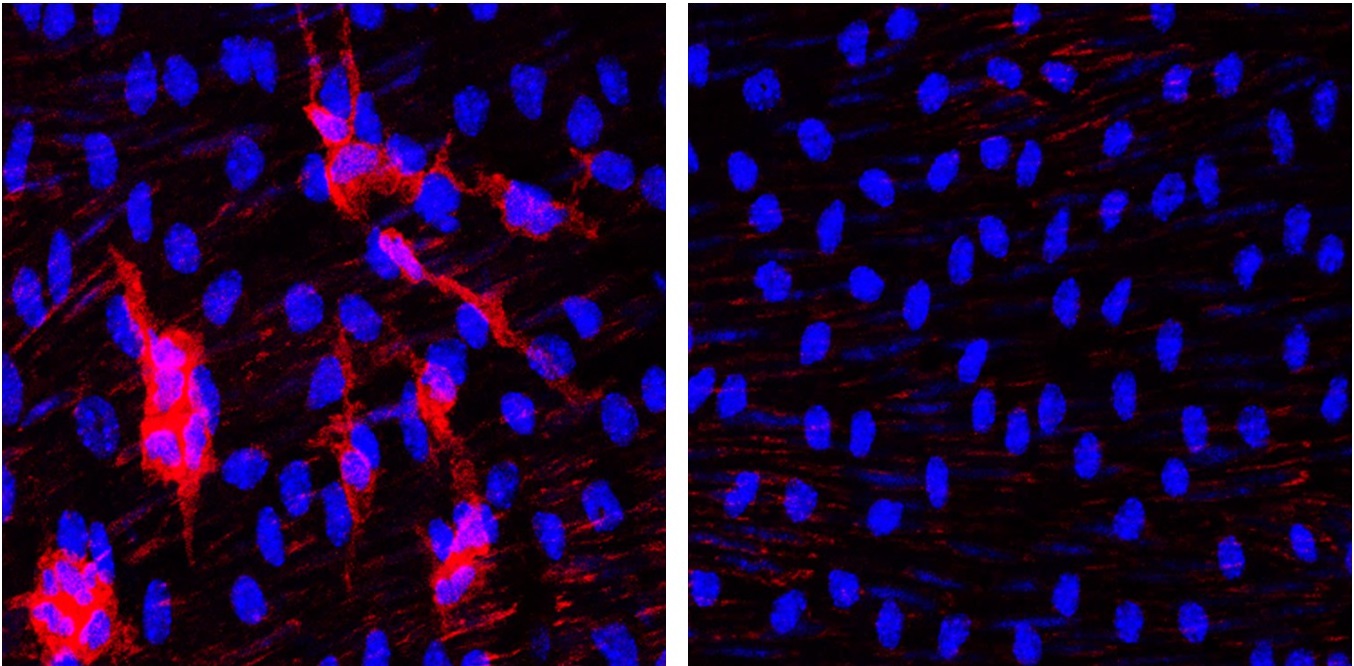
El Dr. Andrés destaca la importancia de investigar en enfermedades raras o minoritarias aunque afectan a un número reducido de pacientes. Según el Dr. Andrés “consideradas globalmente, suponen un problema sanitario-social de gran magnitud, ya que se estima que existen cerca de 7.000 enfermedades raras que afectan al 7% de la población mundial (en España más de 3 millones de pacientes). Dos de los grandes problemas a los que se enfrentan estos pacientes son la falta de diagnóstico y tratamiento adecuados, en gran medida debido a que no se investiga suficientemente sobre estas patologías. En el caso de la progeria, actualmente no hay cura y las terapias paliativas existentes tienen un beneficio limitado. Por ello, es necesario seguir investigando para avanzar en el conocimiento de los mecanismos por los cuales la progerina acelera el envejecimiento y para desarrollar nuevas terapias y, eventualmente, la cura de esta enfermedad”.
Este estudio ha sido posible gracias al apoyo del Ministerio de Ciencia, Innovación y Universidades (MICIU)/Agencia Estatal de Investigación (AEI)/10.13039/501100011033 y ERDF/EU (grants PID2022-141211OB-I00 y PID2022-137111OA-I00); la Comunidad Autónoma de Madrid (grants 2017-T1/BMD-5247 y 2021-5A/BMD-20944) cofinanciado con Fondos Estructurales de Inversión Europeos; RYC2021-033805-I (MICIU/AEI/10.13039/501100011033, European Union NextGenerationEU/PRTR); Ministerio de Educación, Cultura y Deporte; Fundación “la Caixa”; y el Wellcome Trust. El CNIC recibe apoyo del Instituto de Salud Carlos III (ISCIII), del MICIU, de la Fundación Pro-CNIC, y es un Centro de Excelencia Severo Ochoa (CEX2020-001041-S financiado por MICIU/AEI/10.13039/501100011033).











